Enligt en grupp forskare från University of Pennsylvania kan kraften från solen, vinden och havet snart gå samman för att producera miljövänligt vätebränsle. Teamet integrerade vattenreningsteknik i ett nytt experimentellt projekt havsvattenelektrolysator, som använder en elektrisk ström för att separera väte och syre i vattenmolekyler.
Enligt Bruce Logan, professor i miljöteknik vid Kappa och Evan Pugh University professor, kan denna nya metod för "sönderdelning av havsvatten" underlätta omvandlingen av vind- och solenergi till lagringsbara och bärbara bränslen.
"Väte är ett bra bränsle, men du måste få det," sa Logan. – Det enda hållbara sättet att göra detta är att använda förnybar energi och producera den från vatten. Du måste också använda vatten som folk inte vill använda för andra ändamål, och det skulle vara havsvatten. Så väteproduktionens heliga gral var tvungen att kombinera havsvatten, vind och solenergi som finns i kust- och havsmiljöer."
Trots överflöd av havsvatten används det vanligtvis inte för vattenavskiljning. Om vattnet inte avsaltas innan det matas in i elektrolysatorn – ett dyrt extra steg – blir klorjonerna i havsvattnet till giftig klorgas, som förstör utrustningen och sipprar ut i miljön.
För att förhindra detta satte forskarna in ett tunt, semipermeabelt membran som ursprungligen utformats för att rena vatten vid behandling med omvänd osmos (RO). Membranet för omvänd osmos har ersatt det jonbytarmembran som vanligtvis används i elektrolysatorer.
"Tanken bakom omvänd osmos är att du sätter riktigt högt tryck på vattnet, trycker det genom membranet och håller klorjonerna bakom," sa Logan.
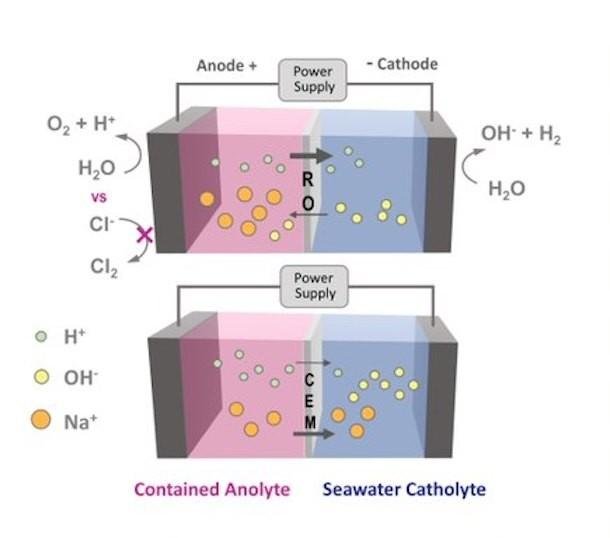
I elektrolysatorn kommer havsvatten inte längre att tränga igenom det omvända osmosmembranet, utan det kommer att hållas kvar av det. Membranet används för att separera reaktioner som sker nära två nedsänkta elektroder – en positivt laddad anod och en negativt laddad katod – anslutna till en extern strömkälla. När strömmen slås på börjar vattenmolekyler dela sig vid anoden, släpper ut små vätejoner som kallas protoner och bildar syrgas. Protonerna passerar sedan genom membranet och kombineras med elektroner vid katoden för att bilda vätgas.
Med ett omvänd osmos-membran installerat stannar havsvattnet kvar på katodsidan och klorjonerna är för stora för att passera genom membranet och nå anoden, vilket förhindrar bildning av klorgas.
Men vid vattenspjälkning, som Logan påpekade, löses andra salter medvetet i vattnet för att göra det ledande. Jonbytarmembranet, som filtrerar joner genom elektrisk laddning, låter saltjoner passera genom det. Det finns inget omvänd osmosmembran.
Eftersom rörelsen av större joner begränsas av RO-membranet, behövde forskarna testa om de små protonerna som rörde sig genom porerna var tillräckligt för att upprätthålla en hög elektrisk ström.
I en serie experiment testade forskarna två kommersiellt tillgängliga omvänd osmosmembran och två katjonbytarmembran, en typ av jonbytarmembran som tillåter förflyttning av alla positivt laddade joner i systemet. Var och en av dem testades för motståndet hos membranet mot jonernas rörelse. Mängden energi som behövdes för att slutföra reaktionerna beräknades också, bildningen av gasformigt väte och syre övervakades, interaktionen med klorjoner och skador på membranet analyserades.
Forskarna fick nyligen ett anslag på $300 000 från National Science Foundation (NSF) för att fortsätta forskningen om havsvattenelektrolys. Logan hoppas att deras forskning kommer att spela en avgörande roll för att minska koldioxidutsläppen över hela världen.
Läs också:
- TSMC: 2021 kommer testkopior av 3nm-processorer att dyka upp
- Tyngdkraften orsakar universums enhetlighet